ニュースリリース
2019年10月03日
武田テバファーマ株式会社
自主回収(クラスI)のお知らせ
H2受容体拮抗剤
ラニチジン錠75㎎・150㎎「タイヨー」/ラニチジン注射液 50㎎・100㎎「タイヨー」
武田テバファーマ株式会社(本社:愛知県名古屋市、CEO兼社長 松森浩士、以下「武田テバファーマ」)は、弊社が製造販売するH2受容体拮抗剤のラニチジン錠75㎎・150㎎「タイヨー」/ラニチジン注射液 50㎎・100㎎「タイヨー」(以下、本製品)につきまして、本日より自主回収(クラスI)を開始いたしました。
本製品の有効成分であるラニチジン塩酸塩に関しましては、先般、海外規制当局において、ラニチジン塩酸塩の製剤および原薬から発がん性物質N-ニトロソジメチルアミン(NDMA)が微量に検出されたことが発表されました。また、国内においては、厚生労働省から9月17日に事務連絡「ラニチジン塩酸塩等における発がん性物質に関する分析について(依頼)」が発出されました。このため、弊社は本製品へのNDMA混入の可能性の調査を開始し、9月20日から本製品の出荷を停止しました。
そして、当該調査の結果、本製品に使用している原薬から管理水準を上回るNDMAが検出されため、有効期限内の全ロットについて自主回収することといたしました。
なお、本製品の安全性に関する社内データからは、これまでに発がん性を示唆する事象は認められておりません。
この度の回収により、患者さんおよび医療関係者の皆様に多大なご心配とご迷惑をお掛けしますことを深くお詫び申し上げます。
以上
記
<回収対象製品 販売名>
ラニチジン錠75mg「タイヨー」
ラニチジン錠150mg「タイヨー」
ラニチジン注射液50mg「タイヨー」
ラニチジン注射液100mg「タイヨー」
<包装規格別対象ロット、数量及び出荷時期>
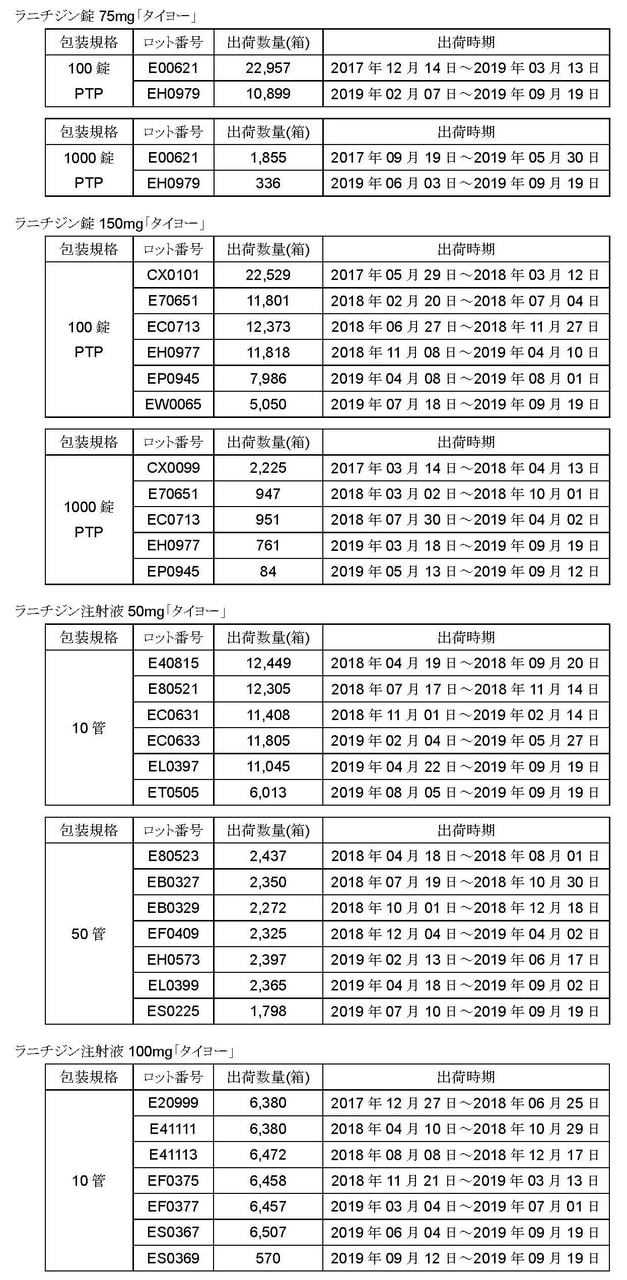
<回収理由>
ラニチジン塩酸塩を原薬とする製剤において、発がん性物質であるN-ニトロソジメチルアミン(NDMA)が検出されたとの海外規制当局の情報を受け、2019年9月17日に厚生労働省から、ラニチジン塩酸塩等における発がん性物質の分析の指示がありました。これを受け、ラニチジン錠およびラニチジン注射液の原薬についてNDMAの分析を実施したところ、管理水準を超えたNDMAが検出されたため、有効期限内の全ロットについて自主回収することといたしました。
<危惧される具体的な健康被害>
NDMAは発がん性物質であり、重篤な健康被害にいたる可能性は否定できませんが、これまでに発がん性を示唆する事象は認められていません。今後、発がん性を示唆する事象が認められた場合はすみやかに情報提供する予定です。
<回収開始日>
2019年10月3日
<効能・効果>
ラニチジン錠75mg・150mg「タイヨー」
胃潰瘍、十二指腸潰瘍、吻合部潰瘍、Zollinger-Ellison症候群、逆流性食道炎、上部消化管出血(消化性潰瘍、急性ストレス潰瘍、急性胃粘膜病変による)
下記疾患の胃粘膜病変(びらん、出血、発赤、浮腫)の改善
急性胃炎、慢性胃炎の急性増悪期
麻酔前投薬
ラニチジン注射液50mg・100mg「タイヨー」
・上部消化管出血(消化性潰瘍、急性ストレス潰瘍、急性胃粘膜病変による)
・侵襲ストレス(手術後に集中管理を必要とする大手術、集中治療を必要とする脳血管障害・頭部外傷・多臓器不全・広範囲熱傷)による上部消化管出血の抑制
・麻酔前投薬
<本件に関するお問い合わせ>
武田テバ ラニチジン錠・注「タイヨー」 専用ダイヤル
TEL:0120-848-281
受付時間 9:00~17:30(土日祝日・弊社休業日を除く。ただし10月5日(土)、6日(日)は対応いたします。)

